中学受験指導専門プロ家庭教師の本郷中学校過去問研究
本郷中学校受験指導はスペースONEのプロ家庭教師にお任せください。
 |
ご依頼専用ダイヤル |
0120-604-405 |
| お問い合わせ(東京本部) |
03-6868-6040 |
| お問い合わせ(福岡校) |
093-592-6658 |
 |
お問い合わせメール
|
|
 |
ws-spaceone |
|
 プロ家庭教師集団スペースONE
プロ家庭教師集団スペースONE
中学受験案内HOME
 インターネット指導コース
インターネット指導コース
2012年度本郷中学校入試問題(過去問) 解答解説
本郷中学校理科過去問研究
2012年度第1回本郷中学校理科入試は配点 75点 試験時間40分
第1回出題内容は 1.化学反応(塩酸と鉄の反応実験) 2.磁力 3.人体(消化)4.光の反射の大問4題構成で例年通り 化学・物理・生物・地学からの1題ずつの出題でした。
第1回理科受験者最高点 58点 受験者平均点 32.2点 合格者平均点 36.4点でした。
今回は 1.塩酸と鉄の反応実験を解説します。
問題1
スペースONEプロ家庭教師の解答で、本郷中学校の発表ではありません。
 本郷中学校・高等学校過去問研究TOPに戻る
本郷中学校・高等学校過去問研究TOPに戻る
(1) 解説解答
⑴ この実験で発生した気体Aの特徴を表しているものを次のア~キからすべて選び、記号で答えなさい。
ア.気体Aにぬれた赤色リトマス紙を近づけると青色に変わる。
イ.気体Aにぬれた青色リトマス紙を近づけると赤色に変わる。
ウ.気体Aを石灰水に通じると白くにごる。
エ.気体Aを試験管に集め、マッチの火を近づけ反応させるとポンと音をたてる。
オ.気体Aのにおいをかぐと、鼻をつくようなにおいがする。
カ.気体Aは水上置換で集めることができる。
キ.気体Aは下方置換で集めることができる。 |
| 解説 |
| 塩酸と鉄が反応して発生する気体は水素です。 |
水素の性質
無色で無臭。水にとけにくい。気体の中で一番軽い。よく燃える。(酸素と水素が混じった気体に点火すると、「ポン」と音をたてて燃える。)
水素が燃えると、空気中の酸素と結びついて水ができる。 (水素+酸素→水)
|
|
| よく燃えるのでエ.気体Aを試験管に集め、マッチの火を近づけ反応させるとポンと音をたてる。。 |
| よって |
| 水に溶けにくいのでカ.気体Aは水上置換で集めることができる。 |
|
| 答 エ カ |
|
|
(2) 解説解答
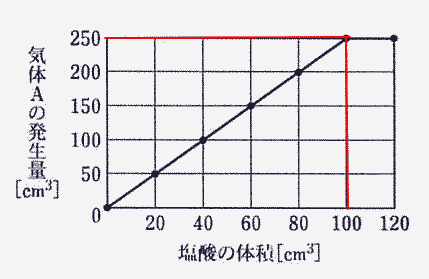
| ⑵ 実験で用いた塩酸120 cm3 と0.77 g の鉄を反応させたときに発生する気体Aの体積は何cm3 ですか。 |
| 解説 |
| 鉄0.55gは塩酸100cm3までと反応するので 鉄0.77gでは 塩酸 100÷0.55×0.77=140cm3まで反応する。 |
| よって 0.77gの鉄は塩酸120cm3と完全に反応する。 |
|
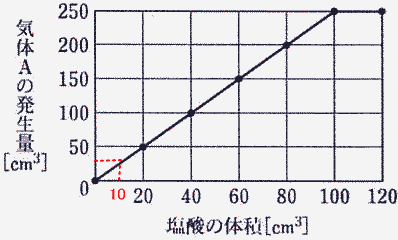
| グラフより 塩酸100cm3で250cm3の水素が発生するから 塩酸1gで 250÷100=2.5g発生する。 |
| よって 塩酸120 cm3では 2.5×120=300 |
|
| 答 300cm3 |
|
|
(3) 解説解答
⑶ 次にさびのついた鉄くぎを用意しました。さびとは鉄が酸化鉄になったもので、5g の鉄がすべて酸化鉄になると重さは6g になります。
用意したさびのついた鉄くぎの重さは1.12 g で、実験で用いた塩酸200 cm3 と反応させると気体Aが400 cm3 発生しました。
酸化鉄は塩酸と反応して気体を発生しないことが分かっています。さびる前の鉄くぎの重さは何g ですか。 |
| 解説 |
|
グラフより 塩酸200cm3が鉄と十分に反応した場合 水素500cm3が発生するので、 水素が400cm3しか発生しなかったので、、鉄と反応した塩酸は 80×2=160cm3
塩酸100cm3と鉄0.55gは十分に反応するので、塩酸160cm3と十分に反応する鉄の重さは 0.55÷100×160=0.88g
よって サビの部分の重さは 1.12ー0.88=0.24g
鉄がさびると 6÷5=1.2倍になるので
サビの部分がさびる前の重さは 0.24÷1.2=0.2g
よって さびのついた鉄くぎ1.12gがさびる前の重さは
0.88+0.2=1.08 |
 |
| 答 1.08g |
|
|
|
(4) 解説解答
| グラフ中の水酸化ナトリウム水溶液40cm3加えたときの混合液にBTB液を数滴たらすと何色になるか答えなさい。 |
| 解説 |
| 塩酸は酸性、ナトリウム水溶液はアルカリ性です。 |
| 酸性の水溶液にアルカリ性の水溶液を少しずつ混ぜると、酸性とアルカリ性がつり合ったところで、中和します。(中性になります)。 |
| BTB(ブロモチモールブルー)液は、、酸性では黄色で、中性では緑色、弱いアルカリ性になると青色に変化します。 |
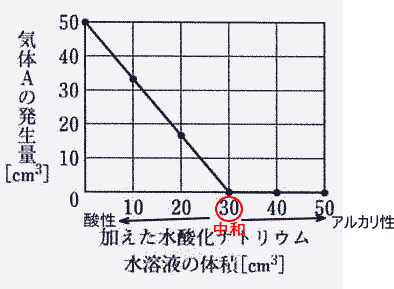 |
| グラフの通り 、加えた水酸化ナトリウム水溶液が30cm3で水素は全然発生しなくなります(中和)。よって水酸化ナトリウム水溶液を30cm3以上加えていくと徐々にアルカリ性が強くなっていきます。 |
|
| 答 青色 |
|
|
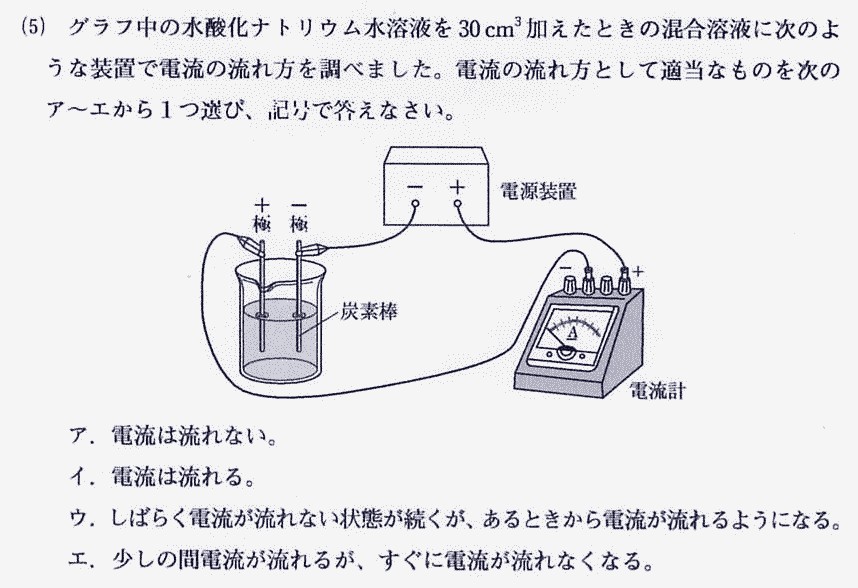
(5) 解説解答
 |
| 解説 |
 |
グラフより 塩酸に水酸化ナトリウム水溶液を30cm3加えると中和します。中性になった水溶液は塩化ナトリウム水溶液(=食塩水)です。
塩化ナトリウム水溶液(=食塩水)は通電性があります。 |
|
| 答 イ |
|
|
(6) 解説解答
| この実験で使用した塩酸50cm3に水酸化ナトリウム水溶液を60cm3加えた混合溶液に十分な量の鉄を反応させたとき、発生する気体Aの体積は何cm3ですか。 |
| 解説 |
|
右のグラフより 水酸化ナトリウム水溶液30cm3に対し塩酸20cm3で中和するので、水酸化ナトリウム水溶液60cm3では塩酸40cm3が中和する。
鉄と反応する塩酸の量は 50ー40=10cm3
|
 |
| 右のグラフより 塩酸10cm3が鉄と反応して水素の量は 50÷2=25(cm3) |
 |
| 答 25cm3 |
|
|
|
HOME
このホームページのすべての文章の文責および著作権はプロ家庭教師集団スペース ONEに属します。